STM:科学家发现了一个能挽救阿尔茨海默病神经元死亡的新策略!
来源:奇点糕 2024-11-12 13:56
该研究证实了,阻断坏死性凋亡过程,不仅可以挽救神经元的死亡,还能在某种程度上改善小鼠的认知功能。
2023年,比利时鲁文大学团队在《科学》上发文,揭示了颗粒空泡变性(GVD)相关坏死性凋亡是阿尔茨海默病(AD)相关神经元死亡的主要原因之一。
近期,该团队又与比利时弗兰德生物技术研究院的科研人员合作发表了一篇文章,进一步确定了tau病理是引发GVD相关坏死性凋亡的关键。而在不同AD小鼠模型中,他们也证实了,使用坏死性凋亡抑制剂(如ponatinib和dabrafenib)阻断坏死性凋亡过程不仅可以挽救神经元的死亡,还能在某种程度上改善小鼠的认知功能。
研究发表在Science Translational Medicine上[1]。

论文首页截图
为了深入分析GVD相关坏死性凋亡与AD主要病理(Aβ病理和tau病理)之间的关系,研究人员构建了多个AD小鼠模型。这些模型包括只表达Aβ病理的APP23转基因小鼠,表达tau病理的TAU22和TAU58小鼠模型,以及同时表达Aβ病理和tau病理的APP23xTAU58小鼠模型。
通过检测坏死执行蛋白pMLKL的表达,研究人员发现,只有在存在tau病理的小鼠模型中才能观察到pMLKL表达升高的现象。
随后通过定量分析这几个表达tau病理的小鼠的神经元数量,研究人员发现,与野生小鼠相比,TAU22和TAU58小鼠的神经元密度明显减少,而APP23xTAU58小鼠的神经元密度减少得更为明显。以上结果表明,GVD相关坏死性凋亡主要与tau病理有关。
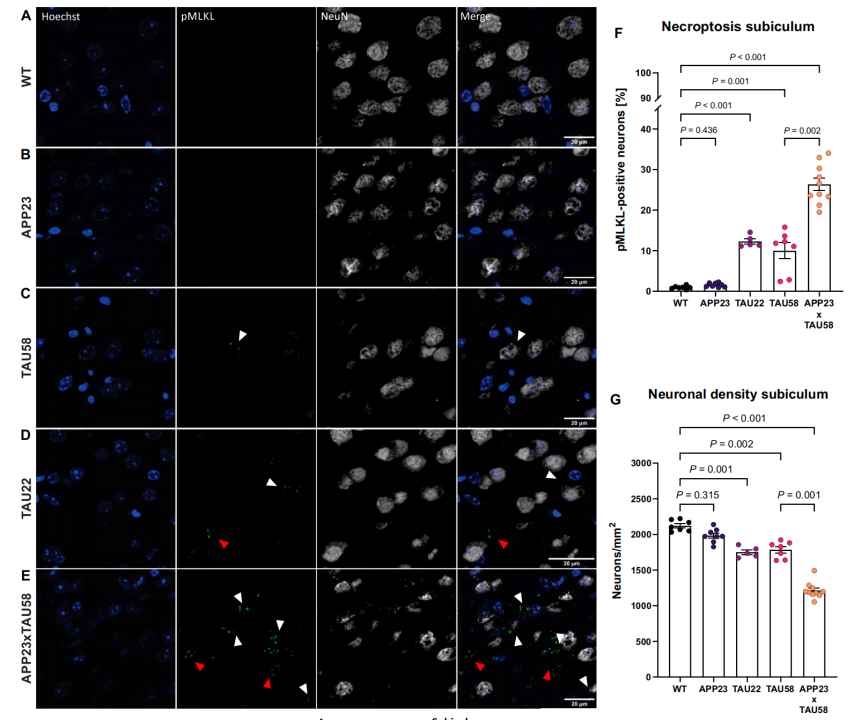
GVD相关坏死性凋亡主要与tau病理有关
接下来,研究人员想进一步明确GVD相关坏死性凋亡与tau病理之间关系。通过检测APP23xTAU58小鼠的神经元内tau蛋白的积累情况,研究人员发现,在APP23xTAU58小鼠中,约有一半以上的pTau阳性神经元中存在pMLKL水平升高的现象,而在野生小鼠模型中则没有观察到这一现象。
这说明,tau病理的存在是引发GVD相关坏死性凋亡的关键。随后的体外研究也证实了这一结果(将小鼠神经元放在从AD患者大脑提取出的tau种子中培养,结果出现了明显的神经元死亡)。
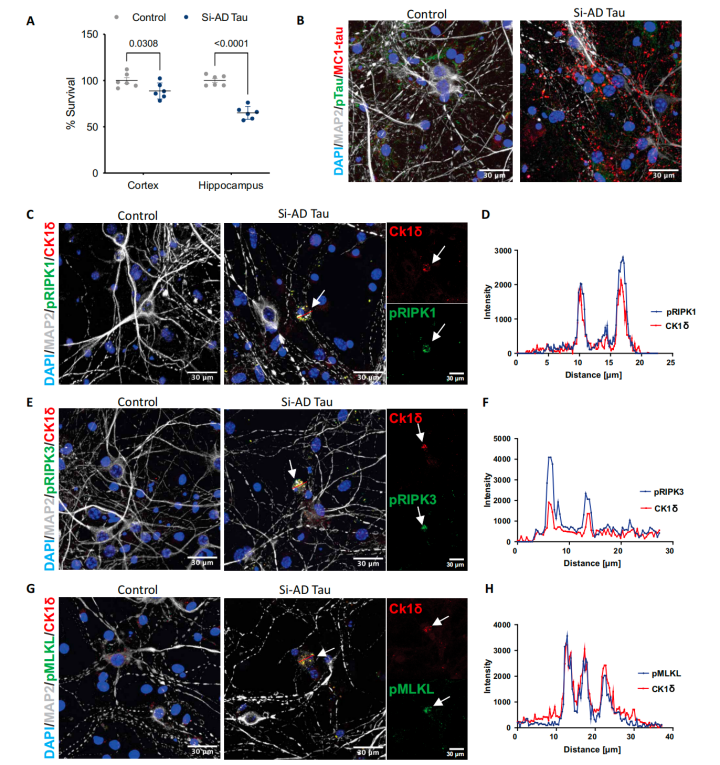
AD脑源性tau蛋白在体外激活小鼠神经元的坏死信号通路
在了解了GVD相关坏死性凋亡与tau病理之间的关系后,研究人员想知道,阻断坏死性凋亡过程,能不能挽救神经元的死亡。
于是,研究人员使用两个特异性靶向坏死性凋亡信号通路的抑制剂,ponatinib(10 mg/kg,腹腔注射)或dabrafenib(30 mg/kg,腹腔注射)来治疗6个月大的APP23xTAU58小鼠。治疗时间共持续16周(每周打5天,歇2天,其中ponatinib是RIPK1和RIPK3抑制剂,已被FDA批准用于治疗急性淋巴细胞白血病和慢性髓细胞性白血病。dabrafenib是一种特异性更强的RIPK3抑制剂)。
结果发现,这两个抑制剂均可以显著降低pMLKL阳性神经元的比例,提高小鼠神经元密度,挽救神经元的死亡。
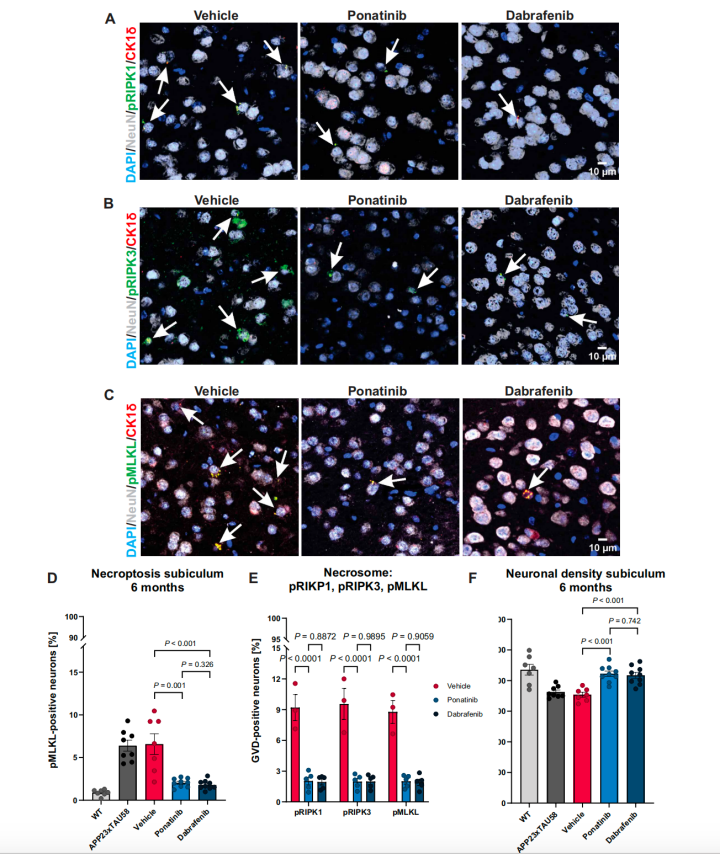
治疗可挽救GVD相关坏死性凋亡导致的神经元死亡
最后,研究人员还测试了接受治疗前后,APP23xTAU58小鼠的认知功能的变化情况。
通过对小鼠进行恐惧条件反射测试(评估学习记忆能力)、T迷宫测试(评估工作记忆能力),以及社交识别测试(评估社交识别记忆能力)后,研究人员发现,治疗可以显著改善小鼠的社交识别记忆能力,但对小鼠的学习记忆能力和工作记忆能力没有显著影响。这也提示,抑制坏死性凋亡过程能在一定程度上对认知功能产生正面影响。
总之,该研究证实了,阻断坏死性凋亡过程,不仅可以挽救神经元的死亡,还能在某种程度上改善小鼠的认知功能。而特异性靶向坏死性凋亡信号通路的抑制剂或许可以作为AD治疗的新策略。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


